Europium, symbolet er Eu, og atomnummeret er 63. Som et typisk medlem af lanthanid har europium normalt +3 valens, men ilt +2 valens er også almindelig. Der er færre forbindelser af europium med en valenstilstand på +2. Sammenlignet med andre tungmetaller har europium ingen signifikante biologiske effekter og er relativt ugiftigt. De fleste anvendelser af europium bruger fosforescenseffekten af europiumforbindelser. Europium er et af de mindst rigelige elementer i universet; Der er kun omkring 5 i universet × 10-8% af stoffet er europium.
Europium findes i monazit
Opdagelsen af Europium
Historien begynder i slutningen af det 19. århundrede: På det tidspunkt begyndte fremragende videnskabsmænd systematisk at udfylde de resterende ledige pladser i Mendeleevs periodiske system ved at analysere det atomare emissionsspektrum. I dag er dette job ikke vanskeligt, og en bachelorstuderende kan udføre det; men på det tidspunkt havde videnskabsmænd kun instrumenter med lav præcision og prøver, der var vanskelige at rense. Derfor blev alle "kvasi"-opdagere i hele historien om opdagelsen af lanthanid ved med at fremsætte falske påstande og diskutere med hinanden.
I 1885 opdagede Sir William Crookes det første, men ikke særlig klare, signal for grundstof 63: han observerede en specifik rød spektrallinje (609 nm) i en samariumprøve. Mellem 1892 og 1893 bekræftede opdageren af gallium, samarium og dysprosium, Paul émile LeCoq de Boisbaudran, dette bånd og opdagede et andet grønt bånd (535 nm).
I 1896 adskilte Eugène Anatole Demarçay tålmodigt samariumoxid og bekræftede opdagelsen af et nyt sjældent jordartselement placeret mellem samarium og gadolinium. Han adskilte med succes dette element i 1901, hvilket markerede afslutningen på opdagelsesrejsen: "Jeg håber at kunne navngive dette nye element Europium med symbolet Eu og en atommasse på omkring 151."
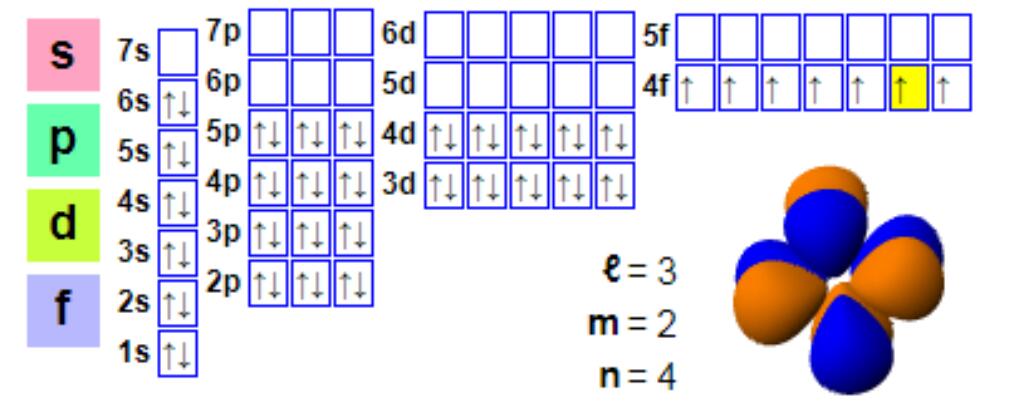
Elektronkonfiguration
Elektronkonfiguration:
1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p66s2 4f7
Selvom europium normalt er trivalent, er det tilbøjeligt til at danne divalente forbindelser. Dette fænomen er forskelligt fra dannelsen af +3 valensforbindelser af de fleste lanthanider. Divalent europium har en elektronisk konfiguration på 4f7, da den halvfyldte f-skal giver mere stabilitet, og europium (II) og barium (II) er ens. Divalent europium er et mildt reduktionsmiddel, der oxiderer i luft for at danne en forbindelse af europium (III). Under anaerobe forhold, især opvarmningsforhold, er divalent europium tilstrækkeligt stabilt og har tendens til at blive inkorporeret i calcium og andre jordalkalimineraler. Denne ionbytningsproces er grundlaget for den "negative europium-anomali", det vil sige, at sammenlignet med forekomsten af chondrit har mange lanthanidmineraler såsom monazit et lavt europiumindhold. Sammenlignet med monazit udviser bastnaesit ofte færre negative europium-anomalier, så bastnaesit er også den vigtigste kilde til europium.
Europium er et jerngråt metal med et smeltepunkt på 822 °C, et kogepunkt på 1597 °C og en densitet på 5,2434 g/cm³. Det er det mindst tætte, blødeste og mest flygtige element blandt sjældne jordarter. Europium er det mest aktive metal blandt sjældne jordarter: ved stuetemperatur mister det straks sin metalliske glans i luften og oxideres hurtigt til pulver. Det reagerer voldsomt med koldt vand for at danne brintgas. Europium kan reagere med bor, kulstof, svovl, fosfor, brint, nitrogen osv.
Anvendelse af Europium
Europiumsulfat udsender rød fluorescens under ultraviolet lys
Georges Urbain, en ung og fremragende kemiker, arvede Demarçays spektroskopiinstrument og fandt ud af, at en yttrium(III)oxidprøve doteret med europium udsendte meget klart rødt lys i 1906. Dette er begyndelsen på den lange rejse for europium-fosforescerende materialer – ikke kun brugt til at udsende rødt lys, men også blåt lys, fordi emissionsspektret for Eu2+ falder inden for dette område.
En fosfor bestående af røde Eu3+, grønne Tb3+ og blå Eu2+-emittere, eller en kombination af dem, kan omdanne ultraviolet lys til synligt lys. Disse materialer spiller en vigtig rolle i forskellige instrumenter verden over: røntgenforstærkende skærme, katodestrålerør eller plasmaskærme, såvel som nyere energibesparende lysstofrør og lysdioder.
Fluorescenseffekten af trivalent europium kan også sensibiliseres af organiske aromatiske molekyler, og sådanne komplekser kan anvendes i forskellige situationer, der kræver høj følsomhed, såsom anti-forfalskning af blæk og stregkoder.
Siden 1980'erne har europium spillet en førende rolle i meget følsom biofarmaceutisk analyse ved hjælp af tidsopløst koldfluorescensmetode. På de fleste hospitaler og medicinske laboratorier er sådan analyse blevet rutine. Inden for life science-forskning, herunder biologisk billeddannelse, er fluorescerende biologiske prober lavet af europium og andre lanthanider allestedsnærværende. Heldigvis er et kilogram europium nok til at understøtte cirka en milliard analyser – efter at den kinesiske regering for nylig begrænsede eksporten af sjældne jordarter, behøver industrialiserede lande, der er paniske over mangel på lager af sjældne jordarter, ikke bekymre sig om lignende trusler mod sådanne anvendelser.
Europiumoxid bruges som stimuleret emissionsfosfor i nye medicinske røntgendiagnosesystemer. Europiumoxid kan også bruges til at fremstille farvede linser og optoelektroniske filtre, til magnetiske boblelagringsenheder og i kontrolmaterialer, afskærmningsmaterialer og strukturmaterialer til atomreaktorer. Fordi dets atomer kan absorbere flere neutroner end noget andet element, bruges det almindeligvis som et materiale til at absorbere neutroner i atomreaktorer.
I dagens hastigt voksende verden kan den nyligt opdagede anvendelse af europium have en dybtgående indvirkning på landbruget. Forskere har fundet ud af, at plastik doteret med divalent europium og univalent kobber effektivt kan omdanne den ultraviolette del af sollys til synligt lys. Denne proces er ret grøn (det er komplementærfarverne til rød). Brug af denne type plastik til at bygge et drivhus kan gøre det muligt for planter at absorbere mere synligt lys og øge afgrødeudbyttet med cirka 10 %.
Europium kan også anvendes på kvantehukommelseschips, som pålideligt kan lagre information i flere dage ad gangen. Disse kan gøre det muligt at lagre følsomme kvantedata i en enhed, der ligner en harddisk, og sende dem over hele landet.
Opslagstidspunkt: 27. juni 2023