Scandium, med grundstofsymbolet Sc og atomnummer 21, er letopløselig i vand, kan interagere med varmt vand og mørkner let i luften. Dens primære valens er +3. Den blandes ofte med gadolinium, erbium og andre grundstoffer med et lavt udbytte og et indhold på cirka 0,0005% i skorpen. Scandium bruges ofte til at fremstille specielt glas og lette højtemperaturlegeringer.
I øjeblikket er de dokumenterede scandiumreserver i verden kun 2 millioner tons, hvoraf 90~95% findes i bauxit-, fosforit- og jern-titanmalm, og en lille del i uran-, thorium-, wolfram- og sjældne jordarters malm, hovedsageligt fordelt i Rusland, Kina, Tadsjikistan, Madagaskar, Norge og andre lande. Kina er meget rigt på scandiumressourcer med enorme mineralreserver relateret til scandium. Ifølge ufuldstændige statistikker er scandiumreserverne i Kina omkring 600.000 tons, som findes i bauxit- og fosforitforekomster, porfyr- og kvarts-wolframforekomster i Sydkina, sjældne jordarters forekomster i Sydkina, Bayan Obo sjældne jordarters jernmalmforekomster i Indre Mongoliet og Panzhihua vanadium-titanmagnetitforekomster i Sichuan.
På grund af manglen på scandium er prisen på scandium også meget høj, og på sit højeste var prisen på scandium oppustet til 10 gange prisen på guld. Selvom prisen på scandium er faldet, er den stadig fire gange prisen på guld!
Opdage historie
I 1869 bemærkede Mendeleev en forskel i atommassen mellem calcium (40) og titanium (48) og forudsagde, at der også var et uopdaget mellemliggende atommasseelement her. Han forudsagde, at dets oxid er X₂OÅ. Scandium blev opdaget i 1879 af Lars Frederik Nilson fra Uppsala Universitet i Sverige. Han udvandt det fra den sorte sjældne guldmine, en kompleks malm, der indeholder 8 typer metaloxider. Han har udvundetErbium(III)oxidfra sort sjælden guldmalm og udvundetYtterbium(III)oxidfra dette oxid, og der er et andet oxid af et lettere element, hvis spektrum viser, at det er et ukendt metal. Dette er det metal, som Mendeleev forudsagde, hvis oxid erSc₂O₃Selve scandiummetallet blev produceret fraScandiumchloridved elektrolytisk smeltning i 1937.
Mendeleev
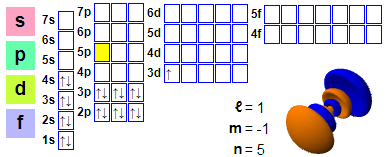
Elektronkonfiguration
Elektronkonfiguration: 1s² 2s² 2p6 3s² 3p6 4s² 3d1
Scandium er et blødt, sølvhvidt overgangsmetal med et smeltepunkt på 1541 ℃ og et kogepunkt på 2831 ℃.
I en betydelig periode efter opdagelsen af scandium blev brugen af scandium ikke demonstreret på grund af dets vanskeligheder i produktion. Med den stigende forbedring af metoder til separation af sjældne jordarter findes der nu en moden proces til rensning af scandiumforbindelser. Fordi scandium er mindre alkalisk end yttrium og lanthanid, er hydroxidet det svageste, så det blandede mineral, der indeholder scandium, vil blive adskilt fra det sjældne jordarter ved hjælp af "trinudfældningsmetoden", når scandium(III)-hydroxid behandles med ammoniak efter at være blevet overført til opløsning. Den anden metode er at adskille scandiumnitrat ved polær nedbrydning af nitrat. Fordi scandiumnitrat er det nemmeste at nedbryde, kan scandium adskilles. Derudover er den omfattende genvinding af ledsagende scandium fra uran, thorium, wolfram, tin og andre mineralforekomster også en vigtig kilde til scandium.
Efter at have opnået en ren scandiumforbindelse omdannes den til ScCl₃Å og smeltes sammen med KCl og LiCl. Den smeltede zink bruges som katode til elektrolyse, hvilket får scandium til at udfældes på zinkelektroden. Derefter fordampes zinken for at opnå metallisk scandium. Dette er et let sølvhvidt metal med meget aktive kemiske egenskaber, som kan reagere med varmt vand og danne hydrogengas. Så metallet scandium, som du ser på billedet, er forseglet i en flaske og beskyttet med argongas, da scandium ellers hurtigt vil danne et mørkegult eller gråt oxidlag og miste sin skinnende metalliske glans.
Applikationer
Belysningsindustrien
Scandiums anvendelser er koncentreret i meget lyse retninger, og det er ikke en overdrivelse at kalde det Lysets Søn. Scandiums første magiske våben kaldes en scandiumnatriumlampe, som kan bruges til at bringe lys til tusindvis af husstande. Dette er et metalhalogenid-elektrisk lys: pæren er fyldt med natriumiodid og scandiumtrijodid, og scandium- og natriumfolie tilsættes samtidig. Under højspændingsafladning udsender scandiumioner og natriumioner henholdsvis lys med deres karakteristiske emissionsbølgelængder. Natriums spektrallinjer er 589,0 og 589,6 nm, to berømte gule lys, mens scandiums spektrallinjer er 361,3~424,7 nm, en række nær-ultraviolette og blå lysudsendelser. Fordi de komplementerer hinanden, er den samlede lysfarve, der produceres, hvidt lys. Det er netop fordi scandiumnatriumlamper har egenskaber som høj lyseffektivitet, god lysfarve, strømbesparelse, lang levetid og stærk dugbrydningsevne, at de kan anvendes i vid udstrækning til tv-kameraer, pladser, sportsarenaer og vejbelysning og er kendt som tredje generations lyskilder. I Kina promoveres denne type lampe gradvist som en ny teknologi, mens denne type lampe i nogle udviklede lande blev udbredt allerede i begyndelsen af 1980'erne.
Scandiums andet magiske våben er solceller, som kan opsamle lys spredt på jorden og omdanne det til elektricitet for at drive det menneskelige samfund. Scandium er det bedste barrieremetal i metalisolatorer, halvledersiliciumsolceller og solceller.
Dets tredje magiske våben kaldes en γA-strålekilde. Dette magiske våben kan skinne klart af sig selv, men denne form for lys kan ikke modtages med det blotte øje, det er en højenergisk fotonstrøm. Vi udvinder normalt 45Sc fra mineraler, som er den eneste naturlige isotop af scandium. Hver 45Sc-kerne indeholder 21 protoner og 24 neutroner. 46Sc, en kunstig radioaktiv isotop, kan bruges som γ-strålingskilde, eller sporstofatomer kan også bruges til strålebehandling af ondartede tumorer. Der er også anvendelser som yttrium, gallium og scandium, granatlaser.Scandiumfluoridglas infrarød optisk fiber og scandiumbelagt katodestrålerør på fjernsyn. Det ser ud til, at scandium er født med lysstyrke.
Legeringsindustrien
Scandium i sin elementære form er blevet brugt i vid udstrækning til dotering af aluminiumlegeringer. Så længe et par tusindedele scandium tilsættes aluminium, vil en ny Al3Sc-fase dannes, som vil spille en metamorfoserolle i aluminiumlegering og ændre legeringens struktur og egenskaber betydeligt. Tilsætning af 0,2%~0,4% Sc (hvilket svarer til andelen af tilsætning af salt til stegte grøntsager derhjemme, kun en lille smule er nødvendig) kan øge legeringens omkrystallisationstemperatur med 150-200 ℃ og forbedre højtemperaturstyrken, strukturel stabilitet, svejseevne og korrosionsbestandighed betydeligt. Det kan også undgå sprødhedsfænomenet, der let kan opstå under langvarigt arbejde ved høje temperaturer. Aluminiumlegeringer med høj styrke og høj sejhed, nye højstyrke korrosionsbestandige svejsbare aluminiumlegeringer, nye højtemperatur aluminiumlegeringer, højstyrke neutronbestrålingsbestandige aluminiumlegeringer osv. har meget attraktive udviklingsmuligheder inden for rumfart, luftfart, skibe, atomreaktorer, lette køretøjer og højhastighedstog.
Scandium er også en fremragende modifikator for jern, og en lille mængde scandium kan forbedre støbejerns styrke og hårdhed betydeligt. Derudover kan scandium også bruges som et tilsætningsstof til højtemperatur wolfram- og kromlegeringer. Udover at lave bryllupstøj til andre har scandium naturligvis et højt smeltepunkt og en tæthed svarende til aluminium, og det bruges også i letvægtslegeringer med højt smeltepunkt, såsom scandium-titaniumlegering og scandium-magnesiumlegering. På grund af sin høje pris bruges det dog generelt kun i avancerede fremstillingsindustrier såsom rumfærger og raketter.
Keramisk materiale
Scandium, et enkeltstående stof, anvendes generelt i legeringer, og dets oxider spiller på lignende vis en vigtig rolle i keramiske materialer. Det tetragonale zirkoniumoxid keramiske materiale, der kan bruges som elektrodemateriale til fastoxidbrændselsceller, har en unik egenskab, hvor elektrolyttens ledningsevne stiger med stigende temperatur og iltkoncentration i miljøet. Krystalstrukturen af dette keramiske materiale kan dog ikke eksistere stabilt og har ingen industriel værdi. Det er nødvendigt at dope nogle stoffer, der kan fiksere denne struktur, for at bevare dens oprindelige egenskaber. Tilsætning af 6~10% scandiumoxid er som en betonstruktur, så zirkoniumoxid kan stabiliseres på et firkantet gitter.
Der findes også tekniske keramiske materialer såsom højstyrke- og højtemperaturbestandig siliciumnitrid som densifikatorer og stabilisatorer.
Som en fortætningsmiddel,Scandiumoxidkan danne en ildfast fase Sc2Si2O7 ved kanten af fine partikler, hvilket reducerer højtemperaturdeformationen af teknisk keramik. Sammenlignet med andre oxider kan det bedre forbedre siliciumnitrids mekaniske egenskaber ved høje temperaturer.
Katalytisk kemi
Inden for kemiteknik anvendes scandium ofte som katalysator, mens Sc2O3 kan bruges til dehydrering og deoxidering af ethanol eller isopropanol, nedbrydning af eddikesyre og produktion af ethylen fra CO og H2. PtAl-katalysatoren, der indeholder Sc2O3, er også en vigtig katalysator til rensning og raffinering af tung oliehydrogenering i den petrokemiske industri. I katalytiske krakningsreaktioner, såsom cumen, er aktiviteten af Sc-Y-zeolitkatalysatoren 1000 gange højere end aktiviteten af aluminiumsilikatkatalysatoren. Sammenlignet med nogle traditionelle katalysatorer vil udviklingsudsigterne for scandiumkatalysatorer være meget lyse.
Atomenergiindustrien
Tilsætning af en lille mængde Sc2O3 til UO2 i nukleart brændsel i højtemperaturreaktorer kan undgå gittertransformation, volumenforøgelse og revnedannelse forårsaget af omdannelse af UO2 til U3O8.
Brændselscelle
Tilsvarende vil tilsætning af 2,5% til 25% scandium til nikkel-alkalibatterier forlænge deres levetid.
Landbrugsavl
I landbruget kan frø som majs, rødbeder, ærter, hvede og solsikke behandles med scandiumsulfat (koncentrationen er generelt 10⁻³ ~ 10⁻⁶ mol/L, forskellige planter vil have forskellig koncentration), og den faktiske effekt af at fremme spiring er opnået. Efter 8 timer steg tørvægten af rødder og knopper med henholdsvis 37 % og 78 % sammenlignet med kimplanter, men mekanismen er stadig under undersøgelse.
Fra Nielsens opmærksomhed på gælden ved atommassedata til i dag, har scandium kun været en del af folks synsfelt i hundrede eller tyve år, men det har næsten ligget på bænken i hundrede år. Det var først med den kraftige udvikling af materialevidenskaben i slutningen af det sidste århundrede, at det bragte ham vitalitet. I dag er sjældne jordarter, herunder scandium, blevet varme stjerner inden for materialevidenskaben, spiller stadigt skiftende roller i tusindvis af systemer, bringer mere bekvemmelighed i vores liv hver dag og skaber økonomisk værdi, der er endnu vanskeligere at måle.
Opslagstidspunkt: 29. juni 2023